Das Tröpfchen-Modell ist eine weitere Möglichkeit den Aufbau eines Atoms zu beschreiben. Hierbei besteht der Atomkern (Nuklid) aus Nukleonen. Es gibt Protonen (positiv [+]) & Neutronen (neutral [n]). Der Atomkern ist positiv geladen.
Abstoßung & Stabilisation im Kern
Wenn im Atomkern doch nur positive und neutrale Ladungsträger sind, müssten die Atomkerne dann nicht zerfallen?
Der Kern des Atoms wird von der sogenannten Kernkraft zusammengehalten. Diese Wechselwirkung innerhalb des Atoms ist sehr groß, aber mit einer kurzen Reichweite. Diese Kraft wirkt wie ein Klebstoff für die Nukleonen.
Schreibweise
^{\text{A}}_{\text{Z}} \text X wobei gilt: \left\{ \begin{matrix} A & = & \text{Massezahl}\\ X & = & \text{Symbol des Atoms/ Isotops}\\ Z & = & \text{Ordnungszahl/ Kernladungszahl/ Protonenzahl}\ \end{matrix} \right.
am Beispiel von Kohlenstoff
Kohlenstoff verfügt als Atom über 6 Protonen und hat eine Massezahl von 12 [siehe Abb. 1].
Schreibweise: ^{12}_6C
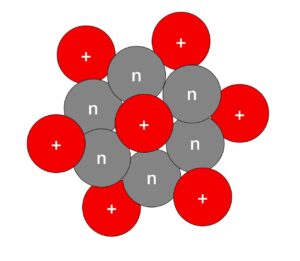
Atome & Isotope
- Isotope sind besondere Atome
- Atome haben gleich viele Neutronen, wie Protonen
- Beispiel: Kohlenstoffatom
- ^{12}_6 C [Abb. 1]
- Isotope zeichnen sich dadurch aus, dass sie nicht gleich viele Protonen wie Neutronen haben
- Beispiel: Kohlenstoffisotop
- ^{14}_6 C
Zusammenfassung
- Atomkern besteht aus Protonen und Neutronen
- Protonen und Neutronen sind Nukleonen (Sg. das Nukleon)
- Massezahl = Anzahl Protonen + Anzahl Neutronen
- Schreibweise:
- Atom: Anzahl Protonen = Anzahl Neutronen
- Isotop: Anzahl Protonen \neq Anzahl Neutronen

No responses yet